Varför får inte alla med Downs syndrom Alzheimers?

Bild från Wikimedia – Amyloid
Erik Portelius, docent vid Göteborgs Universitet, har tillsammans med Henrik Zetterberg, Kaj Blennow och forskare i London och Singapore visat att aktiviteten i genen BACE2 kan vara förklaringen till att cirka 30% av alla personer med Downs syndrom inte utvecklar Alzheimers sjukdom under sin livstid.
Skillnaden mellan en extra kromosom 21 och en extra gen APP
Genen APP ger upphov till de plack i hjärnan som är den första patologiska förändringen i utvecklingen av Alzheimers sjukdom. Personer med Downs syndrom (DS) har en extra kopia av alla gener på kromosom 21 inklusive APP, och cirka 70% av alla personer med DS har utvecklat Alzheimers i 60-årsåldern. Personer som bara har ärvt en extra kopia av genen APP (DupAPP) men inte har Trisomi 21 (T21), har alla utvecklat Alzheimers sjukdom i 60-årsåldern. Det måste alltså finnas någonting på kromosom 21 som också skyddar mot Alzheimers. Forskarna i Göteborg, London och Singapore ville därför undersöka om genen BACE2 kan vara förklaringen.
APP, BACE1 och BACE2
Genen APP kodar för Amyloid Prekursor Protein. Proteinet finns i många vävnader och organ, men särskilt mycket i hjärnan. Proteinet är integrerat i cellmembranet och klipps i flera mindre bitar av olika enzymer. De kortare peptiderna fyller olika funktioner som man inte vet så mycket om. En av peptiderna bildar de plack som leder till Alzheimers sjukdom: amyloid-beta med längden 42 aminosyror (Aβ-42). För att den ska bildas måste proteinet klippas två gånger, först av beta-sekretas och därefter av gamma-sekretas. Beta-sekretas 1, som är den huvudsakliga beta-sekretasen, kodas av genen BACE1 på kromosom 11. Beta-sekretas 2 som kodas av genen BACE2 på kromosom 21 är strukturellt mycket lik BACE1, men dess funktion är inte lika klar.
Undersökning av organoider med Trisomi 21, Disomi 21 och DupAPP
Celler som donerats av 6 personer med Trisomi 21, 1 person med Trisomi 21 Mosaik och 1 person med en extra kopia av APP backades av forskarna till stamceller. De odlades sedan till nervceller som fick bilda tredimensonella organoider. Organoiderna utvecklade hjärnbarkens samtliga sex lager. Från personen med T21 Mosaik odlades två olika cellinjer, en med trisomi och en utan den extra kromosomen (disomi 21).
Patologiska förändringar utvecklades i organoider från 71% av DS-donatorerna
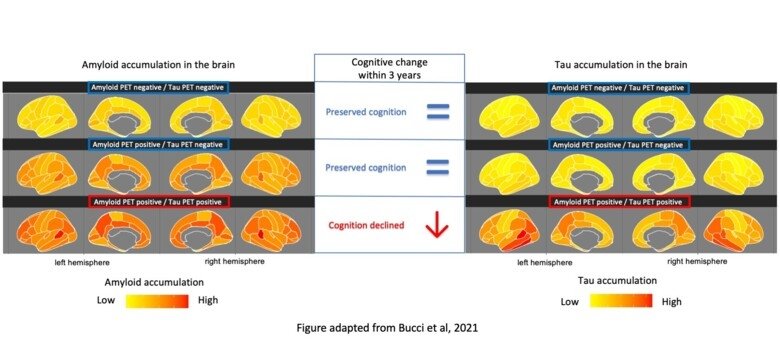
I T21-organoider från 5 av 7 personer (71%) fann forskarna patologiska förändringar i form av fibriller av beta-amyloid utanför cellerna, hyperfosforylerad Tau inne i cellerna, samt tidig förlust av nervceller. Närvaron eller frånvaron av patologiska förändringar var specifik för respektive donator och reproducerades i alla försök.
I de två T21-organoider som inte hade patologiska förändringar klippte man bort den extra kopian av BACE2 med CRISPR/Cas-9, och då utvecklades patologiska förändringar. Dessa kunde förhindras om man samtidigt satte in behandling som inhiberade både beta- och gamma-sekretas.
En extra kopia av BACE2 motverkar skadlig Beta-amyloid på två sätt
BACE1 klyver APP-proteinet, vilket ger upphov till ett ”C-terminalt fragment av APP”. BACE2 kan klippa av detta till en peptid med längden 19 aminosyror, vilket hindrar gamma-sekretas från att klippa av en skadlig peptid med längden 42. BACE2 kan också bryta ned skadlig Beta-amyloid 40/42 till peptider med längden 20 eller 34 aminosyror.
Forskarna visade att den relativa mängden av nedbrytningspeptider (Aβ-20 och Aβ-34) och preventiva peptider (Aβ-19), i förhållande till mängden skadliga peptider, var dubbelt så stor i T21-organoiderna från tre personer, jämfört med såväl D21-organoiden som med DupAPP-organoiden. Tre kopior av BACE2 har alltså en annan effekt än två kopior av BACE2. Den anti-amyloida effekten av BACE2 är dos-beroende. Forskarna jämförde också proportionerna mellan olika peptider i ryggmärgsvätska från personer med DS, och fann motsvarande förhållanden där.
Det fanns också skillnader mellan T21-organoiderna från de tre olika personerna. Andelen förebyggande peptid (Aβ-19) var särskilt stor i T21-organoiderna från en person. Detta kan bero på en s.k. Single Nucleotide Polymorphism (SNP) – en variation i DNA som berör ett enda baspar. SNPs i BACE2 korrelerar med åldern då personer med Downs Syndrom får Alzheimers sjukdom. Individuell variation i BACE2-aktiviteten kan vara en förklaring till att cirka 30% av alla personer med Downs syndrom inte utvecklar Alzheimers sjukdom under sin livstid.

Kliniska försök med BACE1-hämmare påverkar också BACE2
En behandlingsstrategi mot Alzheimers sjukdom som prövas i flera kliniska studier, är att använda ämnen som hämmar aktiviteten i BACE1, för att minska den totala mängden av Beta-amyloid som bildas. Forskarna undersökte två sådana ämnen och visar att de tyvärr också minskar den nedbrytning av skadliga peptider som BACE2 kan åstadkomma.
Sammanfattning
BACE2 är en doskänslig gen som potentiellt förklarar varför cirka 30% av alla personer med Downs syndrom inte utvecklar Alzheimers sjukdom under sin livstid. Studien visar också att organoider med Trisomi 21 kan användas för att screena stora mängder medicin-kandidater, och likaså för att hitta fler gener som skyddar mot neurodegenerativa sjukdomar.
Läs mer:
Patient-specific Alzheimer-like pathology in trisomy 21 cerebral organoids reveals BACE2 as a gene dose-sensitive AD suppressor in human brain. (2020, Jul: Ivan Alić, Pollyanna A Goh, Aoife Murray, Erik Portelius, Eleni Gkanatsiou, Gillian Gough, Kin Y Mok, David Koschut, Reinhard Brunmeir, Yee Jie Yeap, Niamh L O’Brien, Jürgen Groet, Xiaowei Shao, Steven Havlicek, N Ray Dunn, Hlin Kvartsberg, Gunnar Brinkmalm, Rosalyn Hithersay, Carla Startin, Sarah Hamburg, Margaret Phillips, Konstantin Pervushin, Mark Turmaine, David Wallon, Anne Rovelet-Lecrux, Hilkka Soininen, Emanuela Volpi, Joanne E Martin, Jia Nee Foo, David L Becker, Agueda Rostagno, Jorge Ghiso, Željka Krsnik, Goran Šimić, Ivica Kostović, Dinko Mitrečić, LonDownS Consortium; Paul T Francis, Kaj Blennow, Andre Strydom, John Hardy, Henrik Zetterberg, Dean Nižetić.)
PMID32647257, DOI: 10.1038/s41380-020-0806-5 (open access)