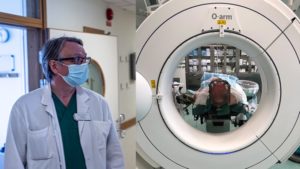
Genom att stimulera hjärnan med en inopererad elektrod blockeras störande signaler och sjukdomar. Metoden kan hjälpa personer som lider av exempelvis Parkinsons sjukdom eller Tourettes syndrom till ett bättre liv. Metoden är inte ny, men en del av den teknik som Skånes universitetssjukhus nu börjat använda sig av är det.
– Tidigare har vi endast kunnat stimulera hjärnan. Nu kan vi även lyssna på den och på så sätt få en inblick i hjärnvågorna och låta dem styra stimuleringen, säger Hjalmar Bjartmarz, överläkare inom neurokirurgin på Skånes universitetssjukhus i Lund.
Skånes universitetssjukhus var ett av de första sjukhusen i världen som använde metoden redan på 1990-talet. Nu är nästa steg taget i utvecklingen, och som första sjukhus i Norden, och det tredje i världen börjar Skånes universitetssjukhus att använda sig av den nya mättekniken.
– Vi har behandlat den tredje patienten i världen med just den här tekniken.
Mätpunkter att orientera sig efter
Metoden Deep Brain Stimulation bygger på en metod där en ram fixerar patientens huvud under operationen och ger neurokirurgen mätpunkter att orientera sig efter i hjärnan. Förenklat handlar det om att hitta exakt det område som orsakar problem i hjärnan. När det är gjort opereras en elektrod in för att blockera störningarna med en nervstimulator. En form av pacemaker.
– Nu när vi även kan lyssna på hjärnan har det blivit lättare att veta var exakt i hjärnan vi ska stimulera, säger Hjalmar Bjartmarz.
Ett bättre liv
Deep Brain Stimulation används i dag för att behandla exempelvis Parkinsons sjukdom, olika skaksjukdomar, dystoni och Tourettes syndrom.
– Min livssituation kommer att bli bättre. Bland annat det sociala. Förhoppningsvis kommer jag att kunna gå ut och äta och ta ett glas vin om jag vill det. Det har varit nästintill helt omöjligt innan, säger Mattias Andersson, som är den första patienten i Norden som fått ta del av den nya Deep Brain Stimulation tekniken.
Bättre behandling för patienten
Karin Wedmark arbetar som sjuksköterska på Deep Brain Stimulation mottagningen på Skånes universitetssjukhus. Hon tror att den nya tekniken kan bidra till att ytterligare förbättra situationen för avdelningens patienter.
– Man kan förhoppningsvis minimera biverkningarna. Det är alltid roligt när det händer nya saker och att man får vara med i den utvecklingen.
För mer information kontakta:
Hjalmar Bjartmarz, överläkare inom neurokirurgi, Skånes universitetssjukhus, 046-17 13 23